造血幹細胞移植・免疫療法グループ
| メンバー | 橋本大吾・荒隆英・大東寛幸・長谷川祐太・豊嶋崇徳 |
|---|
難治性の白血病などに対して、同種造血幹細胞移植は根治を目指せる重要な治療法です。1968年、世界で初めて同種骨髄移植が成功して以来、様々な工夫が行われ移植の安全性・有効性は着実に改善されつつあります。それによって、現在高齢者や合併症を有する症例など、移植の適用は拡大されつつあります。しかしながら、未だ移植関連死亡は根絶されず、免疫チェックポイント阻害剤など移植後の免疫を賦活する治療法の開発もすすみ、移植の安全性を高める必要性はますます高まっています。当研究室では、同種造血幹細胞移植の有効性と安全性を高めるための研究を、マウスモデルと臨床検体を用いて進めています。同種造血幹細胞移植は、ドナー免疫で白血病細胞を根絶する強力な免疫療法であるが (移植片対白血病効果: GVL effect)、近年免疫チェックポイント阻害剤やキメラ抗原受容体T細胞(CAR-T細胞)療法など、新たな免疫療法の開発も進んでいます。こうした免疫療法の発展は多くの腫瘍の治療に応用されているが、やはりその効果には限界がある。本研究室では、こうした免疫チェックポイン阻害剤やキメラ抗原受容体T細胞の作用を増強する新たな治療法の開発を進めています。現在以下のようなプロジェクトが進行中です。
移植片対宿主病(GVHD)の病態生理の解明
造血幹細胞移植法の進歩において、動物実験をはじめとする、基礎研究の役割は非常に大きなものでした。骨髄移植の父であるDonnall Thomasらは、初期の同種骨髄移植の試みが失敗に終わった後、原因を追求するためイヌの骨髄移植モデルを用いて徹底的な基礎研究を行い、ついには移植の成功につなげた事は良く知られています。また、現在世界中で盛んに行われている画期的なGVHD予防法である移植後大量Cyclophosphamide療法も、1980年代に九州大学で行われていたマウス実験に起源を見いだす事が出来ます。このように、動物を用いた同種造血幹細胞移植のモデルは、新しい移植法を開発したり新規薬剤の移植における効果を研究するには最適であり、その結果は着実に臨床の現場に還元されています。こうした研究によって、移植片対宿主病 (graft versus host disease: GVHD)に関して、詳細な細胞・分子学的機序が解明されつつあります (図1)。

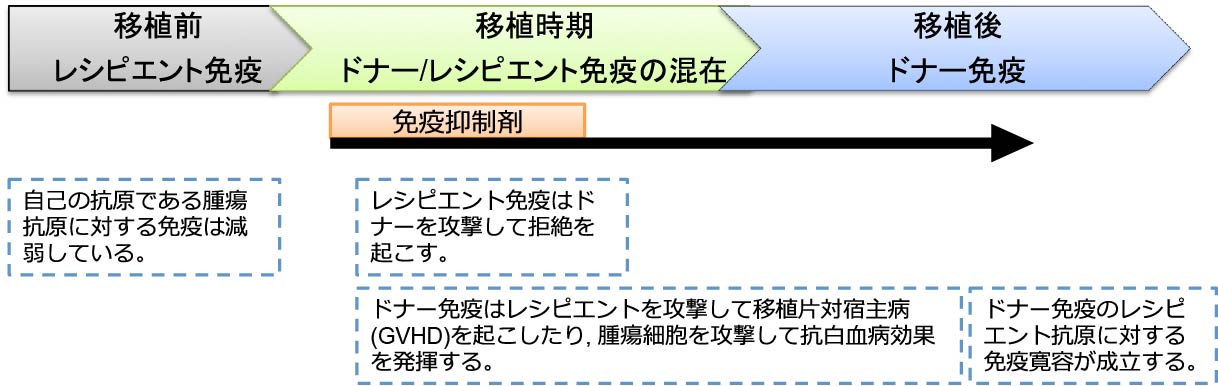
また、造血幹細胞移植は様々な医療行為の中でも、最もDrasticな免疫学的な反応を伴う治療法であり (図2)、移植の研究によって基礎的な免疫学の発見を得ることもあります。
組織幹細胞への炎症記憶とGVHD発症機序の関連
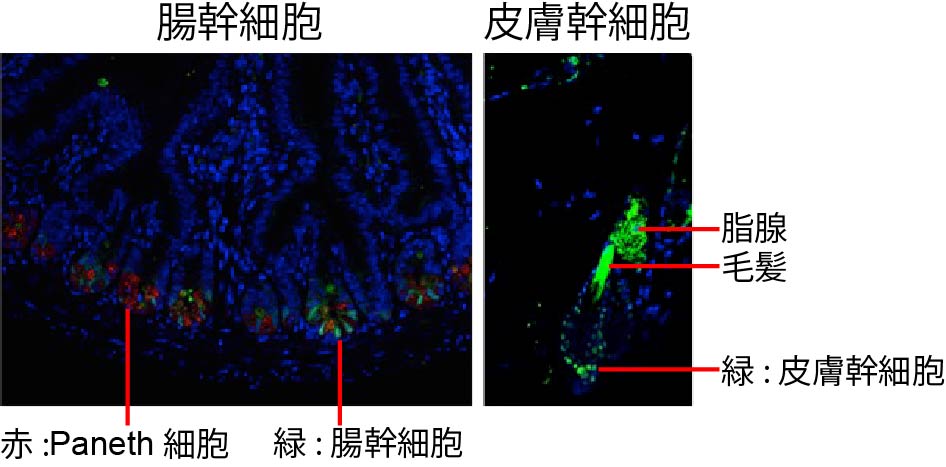
近年、組織には上皮系細胞の組織幹細胞が存在し、種々の上皮細胞に分化して組織の恒常性を維持していることがわかってきました (図3)。私たちのこれまでの研究で、腸管や皮膚の急性GVHDでは、組織幹細胞自体が肝臓の急性GVHDにおける、肝臓の組織幹細胞の役割を解明し、組織幹細胞を標的とする肝臓GVHD予防・治療法の開発を目指して研究を続けています。
組織傷害が生じると、こうした組織幹細胞からの速やかに組織修復が行われ、正常の状態に戻ります。近年、組織修復が終了した後も、炎症の記憶がエピジェネティックな変化として、組織幹細胞に刻まれることが、わかってきています。我々は、GVHDにおける組織損傷・修復後の炎症記憶について、腸管・肝臓オルガノイドを用いて研究を進めています。GVHDが治療抵抗性になる機序の解明を目指しています(図4)。

同種造血幹細胞移植後の疲弊T細胞分化のメカニズムの解明
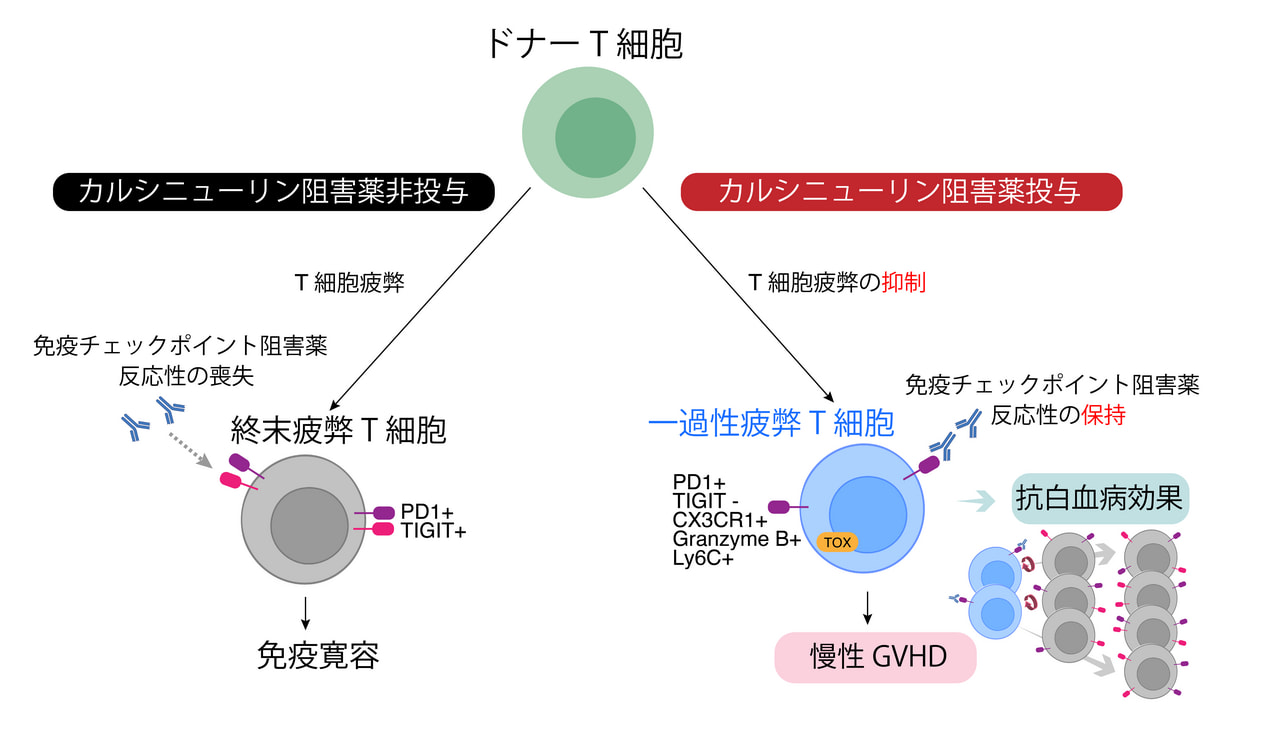
私たちは以前、移植後にドナーT細胞が疲弊T細胞に分化して白血病の再発につながることを発見し、免疫チェックポイント阻害剤が移植後の白血病の再発の抑制に有用であることを世界に先駆けて発見しました(Asakura S, J Clin Invest 2010)。しかしながら、移植後には疲弊T細胞の分化が深く進行するため、免疫チェックポイント阻害剤の効果が減弱することも問題となります。我々は最近、免疫抑制剤であるカルシニューリン阻害剤によって移植後のT細胞疲弊が抑制され、Transitory exhausted T cell (一過性疲弊T細胞)と呼ばれるエフェクター機能を保った特殊な疲弊細胞が増加することをマウスモデルで証明しました (Senjo H: Blood 2023) (図5)。現在は更に研究を進め、患者検体を用いてT細胞のシングルセル解析を行い、臨床の移植におけるTransitory exhausted T cellが、慢性GVHDの発症や移植片対白血病効果の強さを予測するバイオマーカーとなる可能性について検討している。
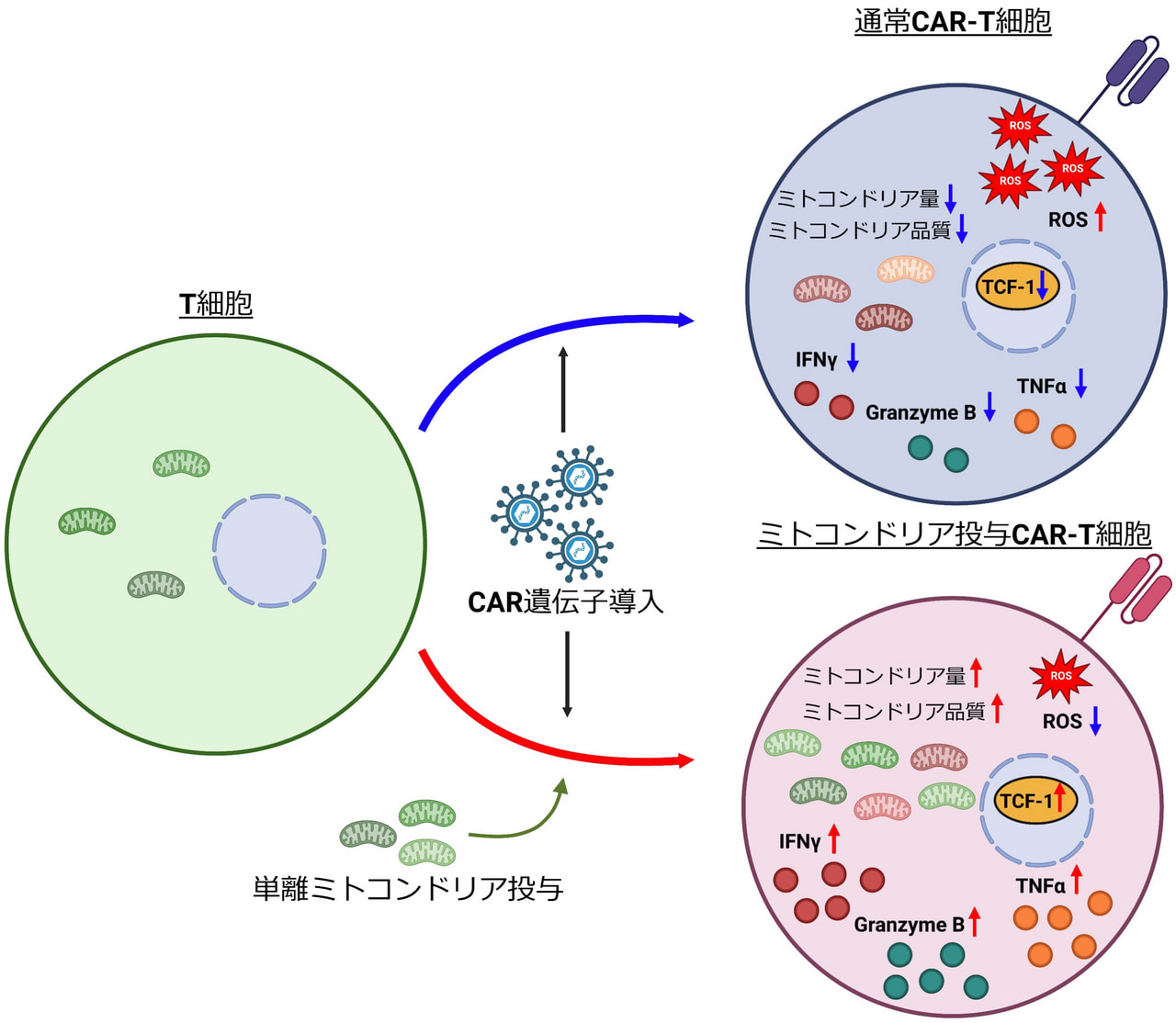
ミトコンドリアナノメディシンを利用した新規CAR-T細胞の開発
同種造血幹細胞移植後やCAR-T細胞療法後などにT細胞が活性化されると、T細胞の活動を支える細胞エネルギーの生成方法は劇的に変化します。さらに、T細胞のエネルギー生成は、T細胞を取り巻く環境 (抗原の多寡、酸素濃度、その他)によっても、大きな影響をうけます。こうしたエネルギー代謝の変化は、移植後の再発やCAR-T細胞の効果不十分の原因と成ることが予想されます。当研究室では、T細胞のエネルギー生成機構を詳細に研究し、T細胞による抗腫瘍効果の増強を目指しています。特に、CAR-T細胞療法の失敗には、CAR-T細胞のミトコンドリアの機能不全が関与することが知られており、機能の保たれたミトコンドリアをCAR-T細胞に移植することによって、CAR-T細胞の効果の増強を目指したい (図6)。